Une séquence de signaux de stress parmi les cellules spécialisées de nettoyage du cerveau pourrait enfin révéler pourquoi certaines réponses immunitaires peuvent provoquer une dégénérescence nerveuse importante entraînant une perte de mémoire, de jugement et de conscience derrière la maladie d’Alzheimer.
Le blocage de cette voie dans le cerveau de souris inspirées de la maladie d’Alzheimer a permis d’éviter d’endommager leurs connexions synapses et de réduire l’accumulation de protéines tau potentiellement toxiques – deux caractéristiques de la maladie.
Les chercheurs, dirigés par une équipe de la City University of New York (CUNY), pensent que cette voie – appelée réponse intégrée au stress (ISR) – provoque des cellules immunitaires cérébrales appelées microglie devenir « sombre » et commencer à endommager le cerveau plutôt qu’à en profiter.
« Nous avons cherché à déterminer quelles sont les microglies nocives dans la maladie d’Alzheimer et comment pouvons-nous les cibler thérapeutiquement », dit Pinar Ayata, neuroscientifique à la CUNY.
« Nous avons identifié un nouveau phénotype neurodégénératif des microglies dans la maladie d’Alzheimer caractérisé par une voie de signalisation liée au stress. »
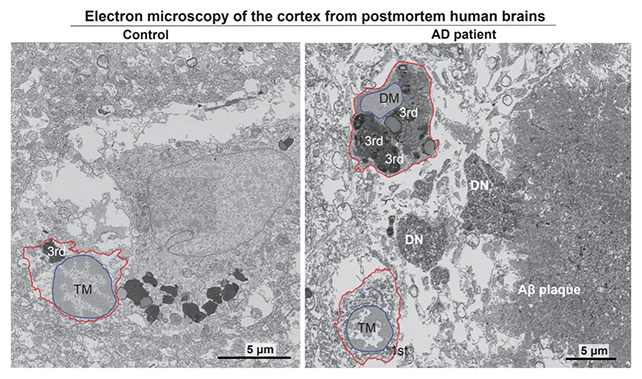
Les cellules immunitaires détraquées ont déjà été lié à la maladie d’Alzheimer, incitant l’équipe à utiliser un processus de balayage électronique pour identifier l’accumulation de microglies sombres dans les cerveaux humains touchés par la maladie d’Alzheimer.
En trouvant environ deux fois plus de microglies stressées dans les cerveaux atteints de cette maladie que dans les cerveaux sains, les chercheurs ont ensuite montré comment la voie ISR provoquait la libération de lipides nocifs par les microglies sombres dans les tissus cérébraux.
Ce sont ces graisses nocives qui ont causé des dégâts synapses et la communication neuronale observée dans la maladie d’Alzheimer.
Comme c’est souvent le cas dans la recherche sur la maladie d’Alzheimer, une meilleure compréhension du fonctionnement de la maladie peut également donner aux scientifiques davantage d’idées sur la manière de la traiter. Si les traitements qui bloquent l’ISR peuvent fonctionner de manière sûre et efficace chez l’homme, la méthode pourrait potentiellement ralentir le chaos provoqué par la maladie d’Alzheimer dans notre propre cerveau.
« Ces résultats révèlent un lien critique entre le stress cellulaire et les effets neurotoxiques des microglies dans la maladie d’Alzheimer », dit la biologiste moléculaire Anna Flury de CUNY.
« Cibler cette voie pourrait ouvrir de nouvelles voies de traitement en arrêtant la production de lipides toxiques ou en empêchant l’activation de phénotypes microgliaux nocifs. »
L’équipe à l’origine de cette étude a découvert que les dysfonctionnements des protéines mal repliées qui conduisent souvent à la démence pourraient déclencher l’ISR, ce qui signifie que ces signaux sont à la fois le résultat de la maladie d’Alzheimer et la raison de sa progression ultérieure.
D’autres études devraient clarifier cette relation, maintenant que nous avons une meilleure idée de la manière dont la voie ISR et les microglies sombres agissent dans le cerveau – et à partir de là, espérons-le, de nouvelles approches thérapeutiques.
« De tels traitements pourraient ralentir considérablement, voire inverser la progression de la maladie d’Alzheimer, offrant ainsi de l’espoir à des millions de patients et à leurs familles », dit neuroscientifique Leen Aljayousi, de CUNY.
La recherche a été publiée dans Neurone.


























